Perjalanan umat manusia dalam memahami struktur atom telah menjadi kisah penemuan yang luar biasa. Di antara para ilmuwan yang berkontribusi terhadap pemahaman ini, Ernest Rutherford berdiri sebagai sosok yang sangat penting. Melalui eksperimen hamburan Rutherford yang terkenal, ia berhasil membuktikan keberadaan inti atom bermuatan positif dan elektron yang bergerak mengelilinginya.
Penemuan ini menjadi tonggak sejarah dalam fisika dan mengubah pandangan kita tentang atom selamanya.
Eksperimen Rutherford yang brilian menggunakan sinar alfa untuk membombardir lembaran tipis emas. Hasilnya menunjukkan bahwa sebagian besar sinar alfa melewati lembaran emas tanpa mengalami defleksi, sementara sebagian kecil lainnya mengalami defleksi yang sangat tajam. Dari hasil ini, Rutherford menyimpulkan bahwa atom memiliki inti yang sangat kecil dan padat, yang bermuatan positif.
Elektron, yang bermuatan negatif, bergerak mengelilingi inti dalam lintasan tertentu.
Ernest Rutherford
Ernest Rutherford, seorang fisikawan kelahiran Selandia Baru, memainkan peran penting dalam penemuan inti atom bermuatan positif dan elektron yang bergerak mengelilinginya. Melalui eksperimen hamburan Rutherford yang terkenal, ia berhasil membuktikan model atom yang sebelumnya diajukan oleh John Dalton dan Niels Bohr.
Eksperimen Hamburan Rutherford
Eksperimen hamburan Rutherford dilakukan pada tahun 1911. Dalam eksperimen ini, Rutherford menembakkan sinar partikel alfa (inti atom helium) ke lembaran tipis emas. Sebagian besar partikel alfa melewati lembaran emas tanpa mengalami defleksi yang signifikan, namun beberapa partikel alfa mengalami defleksi yang sangat besar, bahkan ada yang berbalik arah.
Hasil eksperimen ini menunjukkan bahwa sebagian besar atom emas terdiri dari ruang kosong. Inti atom, yang sangat kecil dan padat, terletak di pusat atom. Inti atom mengandung proton yang bermuatan positif dan neutron yang bermuatan netral. Elektron, yang bermuatan negatif, bergerak mengelilingi inti atom dalam lintasan tertentu.
Struktur Atom Menurut Model Rutherford
Model atom Rutherford menggambarkan struktur atom sebagai berikut:
- Inti atom terletak di pusat atom dan mengandung proton dan neutron.
- Elektron bergerak mengelilingi inti atom dalam lintasan tertentu.
- Sebagian besar atom terdiri dari ruang kosong.
Model atom Rutherford merupakan model atom pertama yang berhasil menjelaskan hasil eksperimen hamburan Rutherford. Model ini menjadi dasar bagi pengembangan model atom modern.
Ilustrasi Eksperimen Hamburan Rutherford
Eksperimen hamburan Rutherford dapat diilustrasikan sebagai berikut:
Seberkas partikel alfa ditembakkan ke lembaran tipis emas. Sebagian besar partikel alfa melewati lembaran emas tanpa mengalami defleksi yang signifikan. Namun, beberapa partikel alfa mengalami defleksi yang sangat besar, bahkan ada yang berbalik arah.
Hasil eksperimen ini menunjukkan bahwa sebagian besar atom emas terdiri dari ruang kosong. Inti atom, yang sangat kecil dan padat, terletak di pusat atom. Inti atom mengandung proton yang bermuatan positif dan neutron yang bermuatan netral. Elektron, yang bermuatan negatif, bergerak mengelilingi inti atom dalam lintasan tertentu.
Elektron
Elektron adalah partikel subatomik yang bermuatan negatif dan merupakan bagian penting dari atom. Mereka ditemukan oleh fisikawan Inggris J.J. Thomson pada tahun 1897, dan sejak itu menjadi pusat studi dalam fisika atom dan kimia.
Elektron memiliki sifat-sifat berikut:
- Muatan: Elektron bermuatan negatif, dengan besar muatan yang sama dengan muatan positif proton.
- Massa: Massa elektron sangat kecil, sekitar 1/1836 massa proton.
- Perilaku dalam Atom: Elektron bergerak mengelilingi inti atom dalam lintasan yang disebut orbital. Orbital ini memiliki tingkat energi yang berbeda, dan elektron dapat berpindah dari satu orbital ke orbital lain dengan menyerap atau melepaskan energi.
Orbital Elektron dan Tingkat Energi
Orbital elektron adalah wilayah di sekitar inti atom di mana elektron kemungkinan besar ditemukan. Orbital memiliki bentuk yang berbeda, dan setiap orbital memiliki tingkat energi yang unik. Elektron menempati orbital dengan tingkat energi terendah yang tersedia, dan mereka dapat berpindah ke orbital dengan tingkat energi yang lebih tinggi dengan menyerap energi.
Orbital elektron dibagi menjadi beberapa tingkat energi, yang diberi nomor dari 1 hingga 7. Tingkat energi pertama, yang paling dekat dengan inti, disebut kulit K. Tingkat energi kedua disebut kulit L, dan seterusnya. Setiap tingkat energi dapat menampung sejumlah elektron tertentu, dan jumlah elektron maksimum yang dapat ditampung oleh tingkat energi tertentu diberikan oleh rumus 2n 2 , di mana n adalah nomor tingkat energi.
Elektron dalam atom dapat berpindah dari satu orbital ke orbital lain dengan menyerap atau melepaskan energi. Ketika elektron berpindah dari orbital dengan tingkat energi yang lebih tinggi ke orbital dengan tingkat energi yang lebih rendah, ia melepaskan energi dalam bentuk foton.
Sebaliknya, ketika elektron berpindah dari orbital dengan tingkat energi yang lebih rendah ke orbital dengan tingkat energi yang lebih tinggi, ia menyerap energi dalam bentuk foton.
Tabel Sifat-sifat Elektron dan Perilakunya dalam Atom
| Sifat | Nilai |
|---|---|
| Muatan | -1,602 x 10-19 coulomb |
| Massa | 9,109 x 10-31 kilogram |
| Kecepatan | 2,188 x 108 meter per detik |
| Orbital | Tingkat energi 1-7 |
| Tingkat Energi | 2n2 elektron |
Model Atom Modern
Model atom Rutherford tidak dapat menjelaskan beberapa fenomena, seperti spektrum atom. Mekanika kuantum, yang dikembangkan pada awal abad ke-20, memberikan penjelasan yang lebih akurat tentang perilaku elektron dalam atom. Model atom modern didasarkan pada mekanika kuantum dan merupakan model yang diterima saat ini.
Peran Mekanika Kuantum dalam Pengembangan Model Atom Modern
- Mekanika kuantum memperkenalkan konsep dualitas gelombang-partikel, yang menyatakan bahwa elektron memiliki sifat gelombang dan partikel.
- Mekanika kuantum memperkenalkan konsep bilangan kuantum, yang merupakan bilangan yang menggambarkan keadaan elektron dalam atom.
- Mekanika kuantum memperkenalkan konsep orbital, yang merupakan daerah di sekitar inti atom tempat elektron kemungkinan besar ditemukan.
Diagram Model Atom Modern
Model atom modern menggambarkan atom sebagai inti atom kecil yang bermuatan positif dan dikelilingi oleh elektron yang bermuatan negatif. Elektron bergerak dalam orbital yang berbentuk seperti awan di sekitar inti atom.
Orbital elektron dibagi menjadi beberapa tingkat energi, dengan tingkat energi yang lebih tinggi terletak lebih jauh dari inti atom. Elektron dapat berpindah dari satu tingkat energi ke tingkat energi lainnya dengan menyerap atau melepaskan energi.
Model atom modern telah berhasil menjelaskan berbagai fenomena, termasuk spektrum atom, ikatan kimia, dan sifat kimia unsur-unsur.
Inti Atom
Inti atom merupakan bagian terkecil dari atom yang terdiri dari proton dan neutron. Proton memiliki muatan positif, sedangkan neutron tidak memiliki muatan. Jumlah proton dalam inti atom menentukan nomor atom unsur tersebut. Nomor atom adalah identitas unik dari suatu unsur dan menentukan sifat kimianya.
Struktur Inti Atom
Inti atom sangat padat dan menempati sebagian kecil dari volume atom. Diameter inti atom sekitar 10^-15 meter, sedangkan diameter atom sekitar 10^-10 meter. Proton dan neutron dalam inti atom diikat oleh gaya nuklir yang kuat. Gaya nuklir ini jauh lebih kuat daripada gaya elektrostatis yang mengikat elektron ke inti atom.
Gaya Nuklir
Gaya nuklir yang mengikat proton dan neutron dalam inti atom adalah gaya nuklir kuat. Gaya nuklir kuat adalah gaya fundamental yang bekerja pada jarak yang sangat pendek, sekitar 10^-15 meter. Gaya nuklir kuat jauh lebih kuat daripada gaya elektrostatis yang mengikat elektron ke inti atom.
Tabel Sifat-sifat Proton dan Neutron dalam Inti Atom
| Partikel | Muatan | Massa (amu) ||—|—|—|| Proton | +1 | 1,007276 || Neutron | 0 | 1,008665 |
Isotop
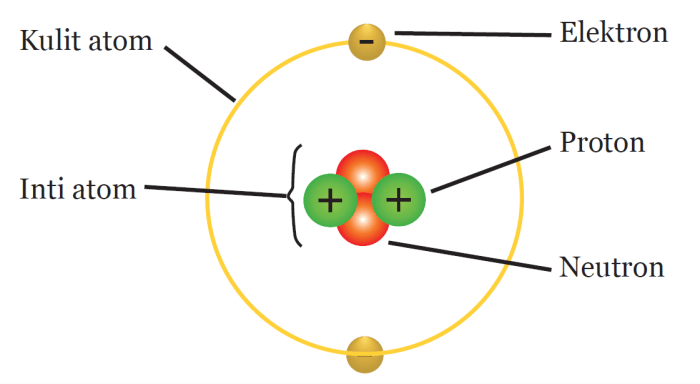
Isotop adalah variasi atom dari suatu unsur yang memiliki jumlah neutron yang berbeda dalam inti atomnya. Jumlah proton dalam inti atom menentukan unsur tersebut, sedangkan jumlah neutron menentukan isotop unsur tersebut. Isotop dapat terbentuk secara alami atau buatan.
Isotop terbentuk ketika sebuah atom memperoleh atau kehilangan neutron. Hal ini dapat terjadi secara alami melalui proses peluruhan radioaktif, atau secara buatan melalui proses reaksi nuklir. Peluruhan radioaktif adalah proses di mana inti atom yang tidak stabil memancarkan partikel untuk menjadi lebih stabil.
Reaksi nuklir adalah proses di mana dua atau lebih inti atom bergabung atau terpisah untuk membentuk inti atom baru.
Contoh Isotop dan Kegunaannya
- Karbon-12: Isotop karbon yang paling umum ditemukan di alam. Digunakan sebagai standar untuk mengukur berat atom.
- Karbon-13: Digunakan dalam pelacak isotop untuk mempelajari proses biologis dan kimia.
- Karbon-14: Digunakan dalam penanggalan radioaktif untuk menentukan usia artefak dan fosil.
- Uranium-235: Digunakan sebagai bahan bakar dalam reaktor nuklir dan senjata nuklir.
- Uranium-238: Digunakan dalam reaktor nuklir sebagai bahan bakar dan sebagai pelindung radiasi.
- Plutonium-239: Digunakan sebagai bahan bakar dalam senjata nuklir.
- Iodine-131: Digunakan dalam pengobatan kanker tiroid.
- Teknesium-99m: Digunakan dalam pencitraan medis.
Sifat-sifat Isotop
- Isotop memiliki sifat kimia yang sama, tetapi sifat fisika yang berbeda.
- Isotop yang berbeda dari suatu unsur memiliki jumlah neutron yang berbeda, tetapi jumlah proton yang sama.
- Isotop yang berbeda dari suatu unsur memiliki berat atom yang berbeda.
- Isotop yang berbeda dari suatu unsur memiliki sifat radioaktif yang berbeda.
Ringkasan Akhir
Model atom Rutherford menjadi dasar bagi perkembangan model atom modern, yang memperkenalkan konsep orbital elektron dan tingkat energi. Penemuan inti atom dan elektron yang bergerak mengelilinginya telah membuka pintu bagi pemahaman yang lebih mendalam tentang struktur materi dan sifat-sifat atom.
Kontribusi Rutherford terhadap ilmu pengetahuan sangatlah besar dan penemuannya terus menjadi landasan bagi penelitian fisika atom dan nuklir hingga saat ini.
Jawaban yang Berguna
Siapakah Ernest Rutherford?
Ernest Rutherford adalah seorang fisikawan kelahiran Selandia Baru yang berkontribusi besar dalam bidang fisika atom dan nuklir. Ia dikenal karena eksperimen hamburan Rutherford yang membuktikan keberadaan inti atom bermuatan positif dan elektron yang bergerak mengelilinginya.
Apa itu eksperimen hamburan Rutherford?
Eksperimen hamburan Rutherford adalah eksperimen yang dilakukan oleh Ernest Rutherford pada tahun 1911. Dalam eksperimen ini, Rutherford menembakkan sinar alfa ke lembaran tipis emas. Hasilnya menunjukkan bahwa sebagian besar sinar alfa melewati lembaran emas tanpa mengalami defleksi, sementara sebagian kecil lainnya mengalami defleksi yang sangat tajam.
Dari hasil ini, Rutherford menyimpulkan bahwa atom memiliki inti yang sangat kecil dan padat, yang bermuatan positif. Elektron, yang bermuatan negatif, bergerak mengelilingi inti dalam lintasan tertentu.
Apa kontribusi Rutherford terhadap ilmu pengetahuan?
Kontribusi Rutherford terhadap ilmu pengetahuan sangatlah besar. Eksperimen hamburan Rutherford-nya membuktikan keberadaan inti atom bermuatan positif dan elektron yang bergerak mengelilinginya. Penemuan ini menjadi dasar bagi perkembangan model atom modern dan membuka pintu bagi pemahaman yang lebih mendalam tentang struktur materi dan sifat-sifat atom.
Rutherford juga dikenal karena karyanya dalam bidang radioaktivitas dan fisika nuklir.






